Βιολογικός παράγοντας βελτιώνει τη ζωή ασθενών με διαπυητική ιδρωταδενίτιδα
Βιολογικός παράγοντας βελτιώνει τη ζωή ασθενών με διαπυητική ιδρωταδενίτιδα
Τα αποτελέσματα της μελέτης PIONEERI δείχνουν ότι οι ασθενείς με μέτρια έως σοβαρή διαπυητική ιδρωταδενίτιδα που έλαβαν adalimumab 40 mg σε εβδομαδιαία βάση πέτυχαν σημαντικά μεγαλύτερη ανταπόκριση τη 12η εβδομάδα σε σχέση με εκείνους, οι οποίοι έλαβαν εικονικό φάρμακο (41,8% έναντι 26%, p = 0,003). Η ανταπόκριση αυτή χαρακτηρίστηκε ως βελτίωση των συνδεόμενων με τη νόσο αποστημάτων και φλεγμονωδών οζιδίων στις 12 εβδομάδες, χρησιμοποιώντας το δείκτη κλινικής ανταπόκρισης στη διαπυητική ιδρωταδενίτιδα (Hidradenitis Suppurativa Clinical Response, HiSCR). Η ανταπόκριση αυτή χαρακτηρίζεται ως μείωση τουλάχιστον 50% από την έναρξη της μελέτης του συνολικού αριθμού των αποστημάτων και των φλεγμονωδών οζιδίων (AN), χωρίς αύξηση του αριθμού των αποστημάτων και των παραγωγικών συριγγίων.
Πιο αναλυτικά, η PIONEERI μία φάσης ΙΙΙ, διάρκειας 36 εβδομάδων, πολυκεντρική, τυχαιοποιημένη, διπλά τυφλή μελέτη, δύο περιόδων, σε ασθενείς με μέτρια έως σοβαρή ΔΙ έγινε σε δύο περιόδους. Στην πρώτη περίοδο της μελέτης διάρκειας 12 εβδομάδων (η λεγόμενη Περίοδος Α), οι ασθενείς τυχαιοποιήθηκαν, ώστε να λάβουν adalimumab 160 mg την εβδομάδα 0, 80 mg την εβδομάδα 2 και 40 mg μία φορά την εβδομάδα (n = 153) ξεκινώντας την εβδομάδα 4, ή εικονικό φάρμακο (n = 154). Μετά την Περίοδο Α, οι ασθενείς μπορούσαν να ενταχθούν σε μια περίοδο θεραπείας 24 εβδομάδων (η λεγόμενη Περίοδος Β). Την Περίοδο Β, οι ασθενείς οι οποίοι αρχικά τυχαιοποιήθηκαν να λάβουν adalimumab, τυχαιοποιήθηκαν εκ νέου να λάβουν adalimumab 40 mg εβδομαδιαία, 40 mg κάθε δεύτερη εβδομάδα, ή εικονικό φάρμακο. Οι ασθενείς οι οποίοι είχαν τυχαιοποιηθεί αρχικά να λάβουν εικονικό φάρμακο ορίστηκαν να λάβουν adalimumab εβδομαδιαία. Το πρωτεύον τελικό σημείο ήταν το ποσοστό των ασθενών που πέτυχαν κλινική ανταπόκριση στις 12 εβδομάδες, χρησιμοποιώντας τον δείκτη HiSCR. Τα αποτελέσματα της Περιόδου B δεν έχουν παρουσιαστεί.3
Οι συχνότερες ανεπιθύμητες ενέργειες (>5% των ασθενών σε οποιαδήποτε ομάδα θεραπείας) που παρατηρήθηκαν στην PIONEERI με το adalimumab έναντι του εικονικού φαρμάκου ήταν επιδείνωση της ΔΙ (9,2% έναντι 13,2%), ρινοφαρυγγίτιδα (5,9% έναντι 10,5%) και κεφαλαλγία (9,2% έναντι 9,9%). Σοβαρές ανεπιθύμητες ενέργειες παρατηρήθηκαν σε 2% των ασθενών υπό adalimumab και σε 3,3% των ασθενών στην ομάδα του εικονικού φαρμάκου.
Τα αποτελέσματα μιας δεύτερης κλινικής μελέτης φάσης ΙΙΙ, της PIONEERII, επίσης για την αξιολόγηση της ασφάλειας και της αποτελεσματικότητας του adalimumab σε ασθενείς με μέτρια ή σοβαρή διαπυητική ιδρωταδενίτιδα, θα παρουσιαστούν σε ένα επερχόμενο ιατρικό συνέδριο.
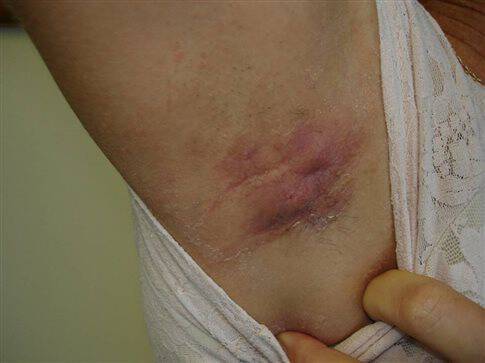
«Τα κλινικά σημεία της διαπυητικής ιδρωταδενίτιδας περιλαμβάνουν οζίδια ή αποστήματα. Αυτά μπορούν να προκαλέσουν σημαντικό πόνο και δυσώδεις εκκρίσεις που μπορεί να ταλαιπωρούν τους ασθενείς», ανέφερε η εξήγησε η Δρ Αλέξα Κιμπαλ, M.D., M.P.H., ερευνήτρια της μελέτης PIONEERI, Ιατρική Διευθύντρια του Οργανισμού Γενικών Ιατρών της Μασαχουσέτης και Καθηγήτρια Δερματολογίας στην Ιατρική Σχολή του Χάρβαρντ. «Τα αποτελέσματα αυτής της μελέτης αποτελούν συνέχεια του έργου που έχει προηγηθεί, αποδεικνύοντας ότι η αδαλιμουμάμπη (adalimumab) μπορεί να μειώσει τα οζίδια και τα αποστήματα σε ασθενείς με μέτρια ή σοβαρή ΔΙ».
health.in.gr



